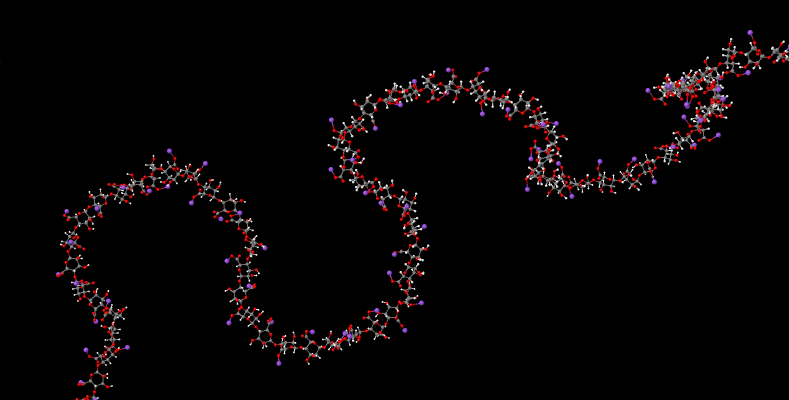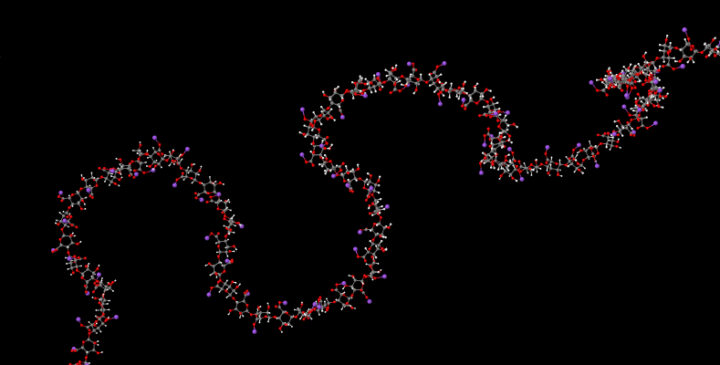
I due acidi mannuronico e guluronico sono due epimeri che differiscono per la configurazione del Carbonio 5 dell’anello dello zucchero.
L’acido guluronico si forma per conversione enzimatica a partire dal mannuronico dopo che è avvenuta la polimerizzazione.
L’acido mannuronico quando polimerizza forma due legami assiali, a differenza del guluronico che forma due legami assiali.
Gli alginati non sono dei copolimeri casuali dei monomeri, ma consistono di blocchi di residui simili e che si alternano strettamente, cioè MMMMMM, GGGGGG and GMGMGMGM, a seconda della fonte algale da cui si estrae.
Si preparano con un vasto campo di pesi molecolari adatti alle varie applicazioni, da 50 fino a 100000 residui.
Si sono dimostrati da tempo biocompatibili, non tossici per le cellule umane, e trovano varie applicazioni dal trattamento alimentare come addensante, biomateriali per tessuti artificiali, per curare le ferite ulcerose, vettore di alcune medicine anticancro e come rimedio contro il riflusso gastroesofageo.
Qui troviamo un del peso molecolare di 24 mila Dalton il cui contro ione è il sodio.
Questo è un primo esempio di alginato ottenuto per polimerizzazione beta 1->4 ell’acido mannuronico. Questo polimero forma legami ad H deboli ed il polimero assume una forma più distesa.
Qui si mostra la posizione dell’acido mannuronico.
Qui si può notare quanto detto sopra sul tipo dei dell’acido mannuronico
Si notino in questa molecola di poliguluronico per prima cosa la formazione dei
Poi si vedano i
Nella molecola di quest’altro polimero dell’acido guluronico è stata inserita una di mannosio. Si perde la linearità della molecola presente nelle altre strutture.
Di seguito ecco un acido poliguluronico che ha come contro ione il Calcio, in verde pisello, che trova posto in un sito formato da cinque ossigeni. Si ruoti la molecola di 90° e si selezionino due atomi di Ca
Si vedano gli Ossigeni in giallo che legano il Calcio : in giallo gli ossigeni in posizione 2 e 3, in violetto quelli degli ioni carbossilati.