La particolarità della Cavilcularina è che essa è dotata di chiralità planare.
E’ la prima molecola naturale che presenta l’attività ottica, cioè è capace di far ruotare il piano della luce polarizzata, a causa di un piano chirale e la sua rotazione della luce polarizzata è di +168.2°.
La chiralità planare, che ha le sue regole per assegnare la configurazione assoluta, è stata finora riscontrata in composti di sintesi particolari come i ciclofani che presentano anelli aromatici con forti tensioni steriche, oppure nel E-ciclottene.
Un piano chirale è un piano di un frammento strutturale in una molecola chirale che non può giacere su un piano di simmetria a causa di una rotazione ristretta dei legami oppure a causa di impedimenti strutturali. Gli enantiomeri di tale molecola chirale differiscono nell’arrangiamento spaziale dei restanti atomi rispetto al piano chirale.
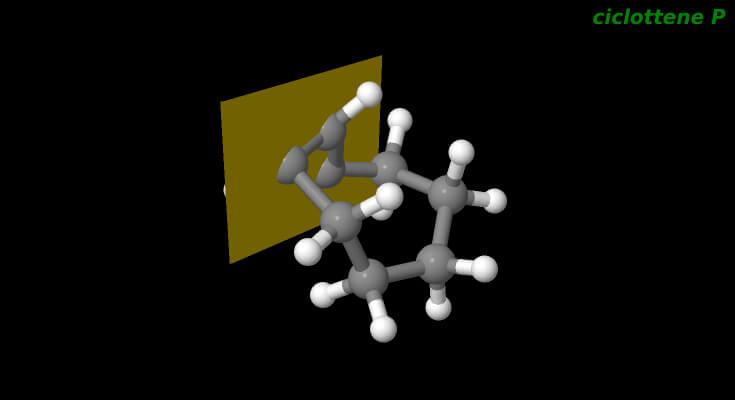
Se consideriamo il caso del cicloottene, l’anello ad 8 atomi di Carbonio permette i due isomeri geometrici.
Uno è il comune Z-ciclottene, l’isomero geometrico trans, mentre l’altro è lo stereoisomero E-ciclottene.
L’analisi teorica sul ciclottene dice che si formano 8 coppie di enantiomeri.
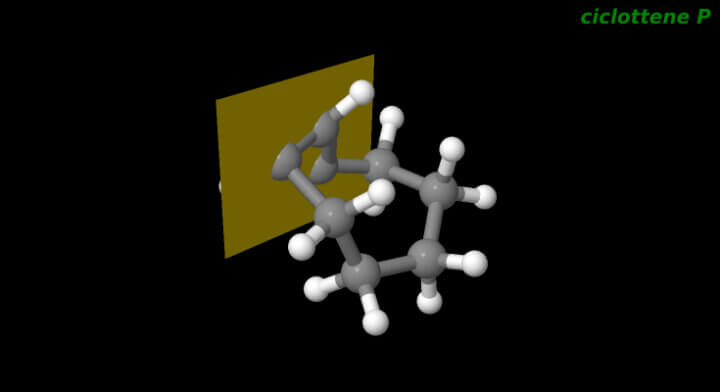
Nell’E-ciclottene gli enantiomeri differiscono per la direzione opposta della rotazione dei loro legami C-C che si trovano di fronte al piano di chiralità, come si può vedere nelle immagini 3d in basso.
Esempi sintetici di molecole dotate della chiralità planare, oltre alla Cavicularia, sono anche la molecola Iorlatinib, un farmaco usato per trattare un carcinoma dei polmoni.
Anche la vancomicina che è un antibiotico e due farmaci macrociclici hanno la chiralità planare.
La rotazione specifica della è di +168.2°. Ha nel suo interno molte tensioni strutturali tra cui un anello benzenico che è piegato di 17° uscendo dalla sua planarità. E’ un angolo che normalmente si ritrova nei ciclofani sintetici.
A queste due strutture ora si deve assegnare la configurazione assoluta secondo le regole di CIP mostrate in questo sito assegnando un descrittore M (Rp) o P (Sp).
In un prossimo articolo mostreremo come si determina la configurazione assoluta con le regole CIP
NB: Purtroppo Jsmol non ci può essere utile nell’assegnazione di questa configurazione assoluta e il pulsante di sotto identifica solo il C=C.
–
Un ulteriore strumento lo trovate qui