Questa proprietà non è caratteristica solo del benzene, oppure di composti idrocarburici ciclici a sei atomi, bensì anche di altre molecole.
La Aromaticità associa una maggiore stabilità termodinamica a struttura di risonanza delocalizzata, stabilità che modera e cambia la reattività di questi composti rispetto agli alcheni tanto da farlo considerare un nuovo gruppo funzionale.
Tale gruppo ha la capacità di modificare anche il comportamento chimico di eventuali altri gruppi ad esso direttamente legati.
Ci sono quattro criteri che devono essere verificati su un sistema π perché possa esserci la proprietà della aromaticità:
- Deve essere un sistema di doppi legami coniugati in cui tutti gli atomi siano ibridizzati sp2 o sp.
- Deve essere un sistema ciclico
- La struttura deve essere planare per permetter una buona sovrapposizione tra gli orbitali atomici p
- Deve essere verificata la regola di Hückel che assegna 4n+2 elettroni, dove n è dato da un numero intero che varia da 0 in poi.
Un sistema per essere aromatico deve verificare tutti e quattro questi vincoli e presenta un orbitale molecolare di tipo π delocalizzato su tutti i centri del sistema π.
Sistemi ciclici coniugati che abbiano invece 4n elettroni π (4, 8, 12 …elettroni) non solo non sono aromatici ma sono anche meno stabili e più reattivi di quanto atteso. Di seguito è presentato il grafico degli Orbitali molecolari di alcuni sistemi ciclici π.
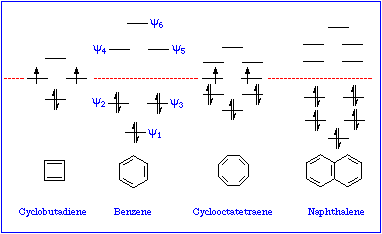
Quando la struttura ciclica presenta un sistema di elettroni π pari a 4n elettroni la regola di Hückel prevede che il sistema sia antiaromatico ed instabile.
Nel 1964 un chimico teorico Heilbronner predisse su basi puramente teoriche che molecole cicliche che avessero una struttura a superficie di Möbius, un anello costruito unendo le estremità di una struttura lineare dopo aver dato una piega, dovessero essere aromatiche se contengono un numero di elettroni π pari a 4n e non 4n+2.
Questa previsione ha stimolato moltissimi a sintetizzare degli idrocarburi aromatici di Möbius che di contro hanno grandi impedimenti sterici da tensione di anello, mentre allo stesso tempo la torsione impedisce la sovrapposizione laterale degli orbitali 2p fondamentale per la delocalizzazione elettronica e la formazione di orbitale delocalizzato.
In sistemi ciclici maggiori la tensione di anello si fa meno pronunciata e le strutture si fanno più flessibili e possono così tornare ad una topologia con meno tensioni secondo le topologie di Hückel.
Finalmente nel 2003 si è riusciti a sintetizzare un composto simile che combina un sistema con orbitali p ortogonali all’anello del piano e una struttura aromatica a striscia come un composto di Möbius stabilizzato dal sistema esteso π.
La molecola sintetizzata era un 16 annulene che secondo il chimico inglese Henry Rzepa possiede anche la chiralità assiale, non avendo alcun elemento di simmetria che impedisca la chiralità, e possiede un’attività ottica calcolata di -1355°.
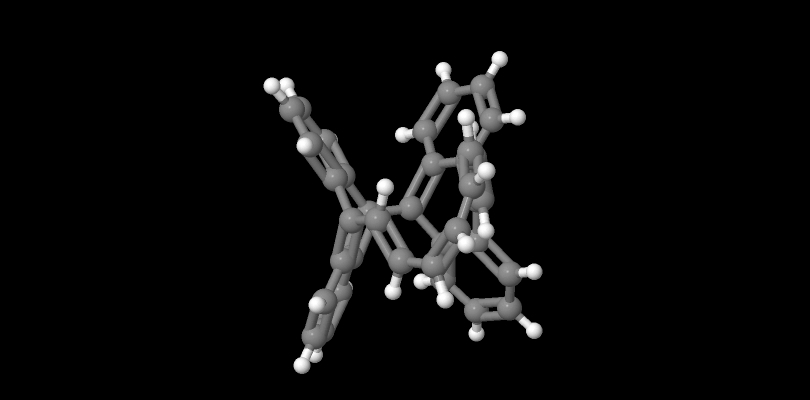
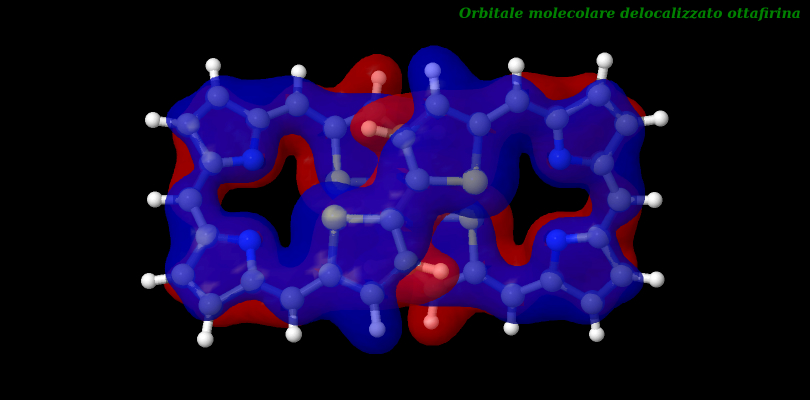
In un altro articolo lo stesso chimico inglese esplora un composto della classe dei ciclopolipirroli, Firine, che oltre a presentare la chiralità assiale e la rotazione ottica associata, presenta anche un orbitale molecolare delocalizzato a conferma della aromaticità
Sistemi aromatici ed antiaromatici di Hückel
La molecola del 1,3,5,7-cyclooctatetraene è presente in due conformazioni: una non è planare ed adotta una conformazione a tubo; si comporta chimicamente come un alchene; per idrogenazione completa forma il cicloottano. L’altra è planare ed è antiaromatica e si comporta anch’essa come un alchene.
Il ciclobutadiene in realtà non è mai stato isolato e se ne è verificata la presenza solo in fase gassosa.
Si noti come nei sistemi del ciclobutadiene e del cicloottatriene vi siano due elettroni spaiati che hanno un’energia pari agli orbitali P di partenza. Molecole simili sono definite ANTIAROMATICHE.
e. Queste molecole sono il riferimento per la reattività dei successivi. Il avendo due elettroni spaiati, si comporta come molecola antiaromatica, molto meno stabile del diene di partenza. In effetti il ciclobutadiene non è stabile. Se invece leghiamo quattro gruppi terz Butile, , si impedisce che i due elettroni spaiati siano disponibili verso altri reagenti e la molecola diventa stabile.Il cicloottariene ha due isomeri, uno a forma tubolare, l’altro a forma planare. Entrambe queste due molecole hanno una bassa stabilizzazione termodinamica e si comportano come degli alcheni
Composti aromatici di Hückel
Orbitale Pgreca a più bassa energia, OCCUPATO, delocalizzato su tutta la molecola.
Orbitale Pgreca di AntiLegame (LUMO)- Orbitale Pgreca di Legame.
Di seguito viene mostrata la superficie di densità elettronica calcolata sulla superficie di Van Der Walls e su una distanza a 80% della distanza di Van Der Walls
Composti aromatici di Möbius
–
Il pirrolo quando viene fatto polimerizzare forma composti chiamati porfirine di cui il gruppo eme è un esempio.
–