La Enolasi è classificata come una liasi, una idrolasi, che rompe il legame ossigeno carbonio.
L’enzima della glicolisi si chiama 2 fosfoDglicerato idrolasi (che forma il PEP)
2-fosfo-D-glicerato ⇌ Fosfoenolpiruvato + H2O
L’energia libera standard biologica della reazione è leggermente positiva e si trova quindi in condizioni di equilibrio, ΔG’°=+1,8 kJ/mole. Se il fosfoenolpiruvato perciò è successivamente idrolizzato per produrre ATP la reazione di formazione va avanti.
Perché l’enolasi possa esplicare la sua azione ha bisogno di un catione bivalente, come Zn2+, Mn2+ e Co2+, che attivano o disattivano l’enzima.
Il Magnesio ione determina molto la cinetica dell’enzima stesso.
Fu scoperto nel 1934 ed è presente in tutti i tessuti ed organismi che possono fare la glicolisi.
Negli esseri umani ci sono tre subunità di enolasi, alfa, beta e gamma, codificate in tre geni differenti, che si possono combinare a dare cinque tipi di isoenzimi differenti, ma solo tre sono i più comuni che si trovano nelle cellule dell’uomo.
Alfa-alfa, o anche enolasi non neunorale o ENO1 che si ritrova in tutte le cellule dell’uomo.
Beta-beta oppure enolasi specifica del muscolo ed è la ENO3 e si trova ad alti livelli nel muscolo.
Gamma-Gamma è l’enolasi specifica dei neuroni, ENO2. Nei neuroni è espressa moltissimo fino a rappresentare il 3% delle proteine totali solubili. (Link)
Un inibitore della enolasi è lo ione Floruro per la sua capacità di complessare il 2PG ed il Mg2+ bloccandone l’attività.
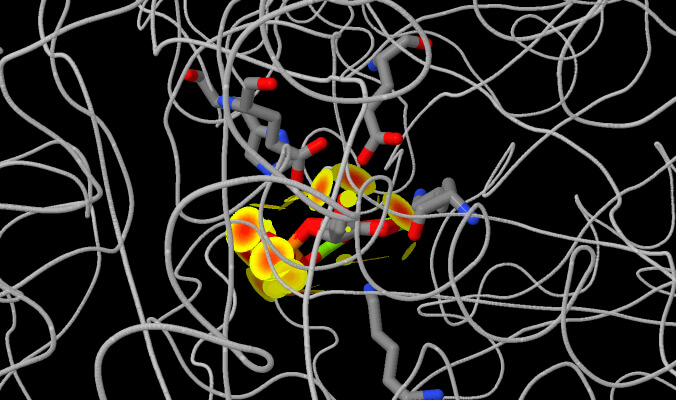
MOLECOLE NEL SITO ATIVO
– – –
Si noti che in questa visualizzazione 2PG e PEP sono sovrapposti per far vedere come cambi di pochissimo la loro disposizione
SITO ATTIVO
Il sito attivo dell’enolasi coinvolge gli amminoacidi Lys 345, Lys 396, Glu 168, Glu 211, e His 159 di ogni subunità