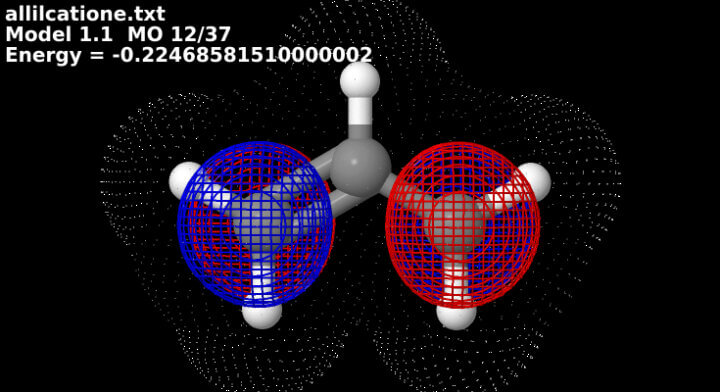
La prima è calcolata e disegnata sulla superficie di Van Der Walls, mentre la seconda ad una distanza minore dai nuclei e rappresenta una distribuzione più reale delle cariche.
Gli orbitali LUMO sono gli orbitali molecolari non occupati a più bassa energia; mentre HOMO sono gli orbitali molecolari occupati a più alta energia.
Sono in pratica gli orbitali che definiscono la reattività di una molecola. Per orbitale delocalizzato si intende l'orbitale molecolare Pgreca che si estende su tutti i centri e che definisce la struttura della risonanza.
Prima di tutto si misurino le lunghezze di legame e l’angolo di legame. Le lunghezze si trovano uguali a 0,137 nm per tutti e due i legami C-C, mentre l’angolo di legame è di 119,3°. Negli alcheni la lunghezza di legame è di 0,131, mentre nel legame tra doppio legame e CH3 è 0,148.
La giustificazione di queste lunghezze di legame la si trova negli orbitali del carbocatione allilico, specie nell’orbitale delocalizzato, e nella distribuzione della carica positiva sui C nelle MEP.