La corrispondente parte teorica degli O.M. la potete esaminare alla sezione teorica
Dal quadro energetico degli orbitali molecolari si deduce il comportamento chimico di questi due importanti gas così vitali per la vita sulla terra.
L’azoto N2 è un gas inerte e pochissimo reattivo, mentre l’Ossigeno O2 è tanto attivo da non poter permettere la vita se non è miscelato con gas inerti a causa del suo doppietto esterno che è molto reattivo.
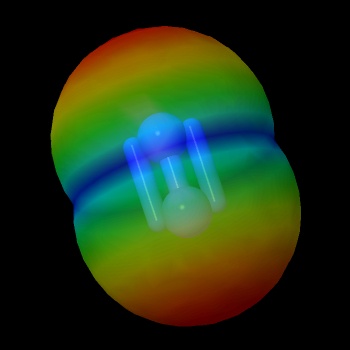
 Per il quadro generale degli orbitali molecolari delle molecole biatomiche si veda questo articolo. Si notino come l’ultimo orbitale occupato sull’azoto sia di legame e si estende anche tra i nuclei; quello molecolare occupato (HOMO) dell’ossigeno è di antilegame in quanto l’orbitale si concentra fuori dalla zona internucleare.
Per il quadro generale degli orbitali molecolari delle molecole biatomiche si veda questo articolo. Si notino come l’ultimo orbitale occupato sull’azoto sia di legame e si estende anche tra i nuclei; quello molecolare occupato (HOMO) dell’ossigeno è di antilegame in quanto l’orbitale si concentra fuori dalla zona internucleare.
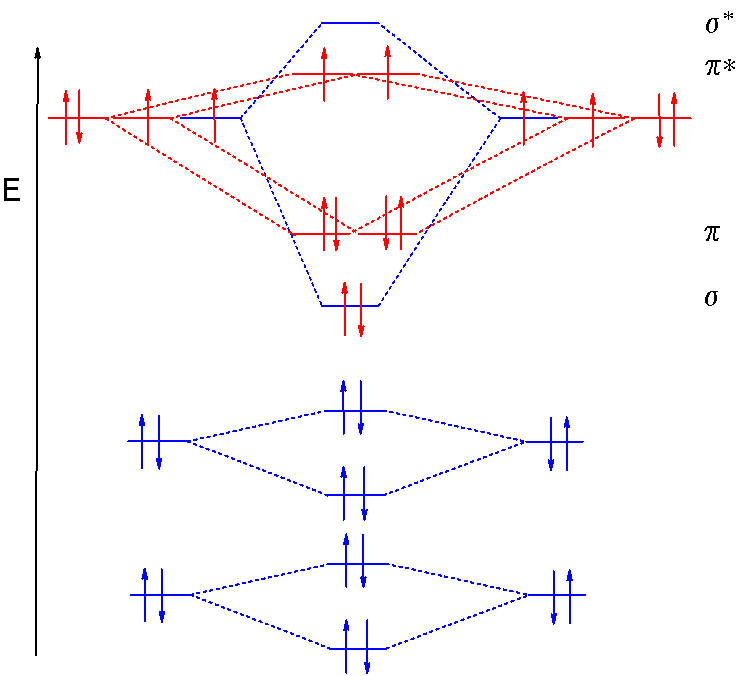
Proprio il quadro energetico degli orbitali molecolari dell’Ossigeno spiega il Paramagnetismo della molecola a causa dei due elettroni spaiati su due orbitali Pgreca di antilegame. Wikipedia
ORBITALI MOLECOLARI OSSIGENO
ORBITALI MOLECOLARI AZOTO