Una delle sintesi importanti della Chimica Organica è la trasformazione tra alcoli, aldeidi e chetoni mediante reazione di ossidazione e riduzione.
Gli agenti riducenti importanti usati per la riduzione da ALDEIDE O CHETONE ad ALCOL sono due: Boridruro di Sodio, NABH4, e Idruro di Litio ed Alluminio, LiAlH4, e loro varianti.
Il Boridruro di sodio (NaBH4) è un composto ionico in cui la carica negativa è sul gruppo tetraidroborato capace di donare al Carbonile uno ione IDRURO H-.
Il gruppo carbonile delle aldeidi e chetoni è quindi trasformato in alcol primario se si parte dall’aldeide, secondario se si parte dal Chetone. Qualora si vuole sintetizzare un alcol terziario bisogna usare i reagenti di Grignard
Finché in una molecola organica esiste un solo gruppo funzionale da ridurre, i due reagenti NaBH4 e LiAlH4 sono equivalenti. Quando invece si hanno più gruppi che possono interagire bisognerà scegliere il reagente opportunamente tenendo conto la principale differenza tra i due è la forza basica.
Gli acidi carbossilici decompongono il boridruro col proprio idrogeno acido e per questo non possono essere ridotti ad aldeide.
LiAlH4 è un riducente più ENERGETICO del NaBH4 e non può essere usato in presenza di H acidi (di alcol, ammine, acidi) e deve essere usato in solvente aprotico come THF. In una seconda fase si acidifica il prodotto di reazione.
Un altro modo di portare avanti la reazione prevede l’uso di solvente come DIGLIMA e aggiunta di NaOH al 15% seguita da un’aggiunta di acido diluito per neutralizzare e separare il prodotto.
NaBH4 invece è più debole e lo si usa in presenza di alcol metilico o etilico solo per aldeidi e chetoni a cui segue un’acidificazione con acido diluito ed eventuale separazione. Un esempio può essere la riduzione di un chetone e/o aldeide alfa-beta insaturo in cui si riduce il carbonile senza toccare il doppio legame C=C.
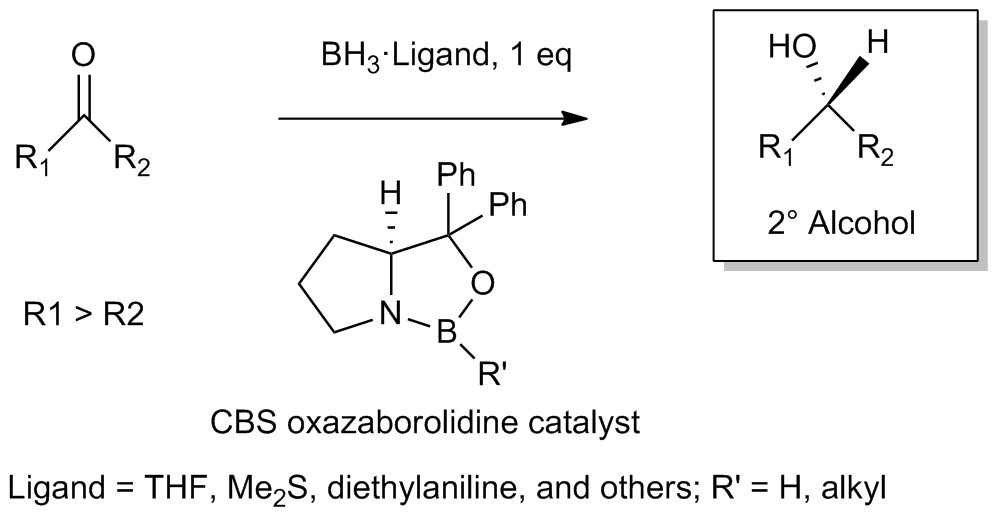
La riduzione delle aldeidi e chetoni assume una grande importanza quando i composti che si vogliono ottenere sono alcoli chirali, in quanto il diverso ingombro sterico dei gruppi sul chetone e sull’agente riducente, o la presenza di catalizzatori anch’essi chirali come Oxazaborilidina, possono far decorrere la reazione verso un alcol chirale. Si veda
Il meccanismo di RIDUZIONE con NaBH4 è il seguente:
Il meccanismo di riduzione di un carbonile da parte del NaBH4 che qui illustriamo è una semplificazione del processo reale.
In una prima fase individuiamo i centri di reazione: lo Ione BH4- è un donatore di uno ione Idruro, di un idrogeno col suo doppietto.
Lo ione idruro entra sul C del Carbonile che ha una parziale carica positiva per la presenza dell’Ossigeno e si forma uno
Si noti come la carica negativa iniziale del boridruro ora sia condivisa con l’ossigeno del carbonile.
Nella fase successiva lo Stato di Transizione evolve verso la formazione del prodotto
–
Nella fase successiva poiché il solvente usato è in genere un alcol metilico o etilico, si acidifica l’alcossido con un acido diluito per protonare l’alcolato e liberare l’alcol relativo.
Il meccanismo qui prodotto in realtà è esemplificativo perché non tiene conto dell’aiuto offerto dai protoni del solvente nella stabilizzazione della carica che si forma. In solventi aprotici questa riduzione non si ha infatti.