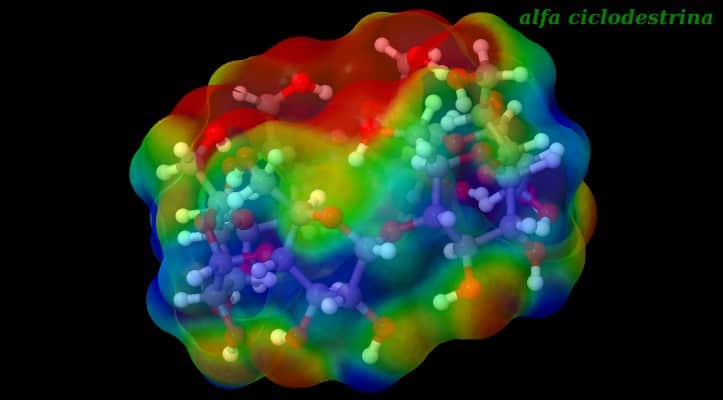
Le ciclodestrine formano dei composti di inclusione solubili con molecole meno idrofile che si possono arrangiare dentro la lora cavità.
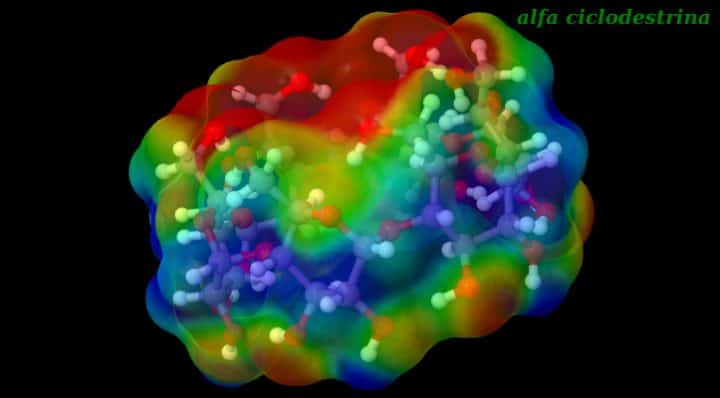
Ci sono tre tipi di ciclo-destrine di seguito presentate che si formano per condensazione di 6 (AlfaCD), 7 (beta CD) , 8 (gamma CD) molecole di residui D-glucopiranosio, legate tra loro mediante legami α-1,4 glicosidici.
Tutti gli anelli di glucosio hanno una conformazione a sedia presente in tutte le molecole di alfaciclodestrine a meno di tensioni di anello per dover accomodare un diverso numero di residui.
La struttura complessiva è quella di un tronco di cono irrigidita da legami ad IDrogeno tra i gruppi 2-OH e 3-OH sul bordo più esterno.
Le forze dei legami ad Idrogeno variano col numero di molecole di glucosio secondo
α-ciclodestrine < β-ciclodestrine < γ-ciclodestrine.
I gruppi 6OH sono anche capaci di dare legami ad idrogeno lungo l'orlo inferiore ma sono destabilizzati da effetti dipolari, facilmente dissociati in soluzioni acquose e non ritrovati tipicamente nei cristalli delle ciclo-destrine.
Il legame ad Idrogeno è tutto 3-OH donatore e 2-OH accettore nelle alfaciclodestrine ma cambia verso 3-OH accettore 2OH- donatore nelle beta e gammaciclodestrine.
A seconda del numero di molecole di glucosio condensate, la cavità ha dei diametri crescenti, misurabili tra gli Ossigeni anomerici opposti, mentre la profondità dei tronchi di cono resta la stessa, attorno ai 0.8 nm.
Gli anelli delle ciclodestrine sono anfipatici: le superfici interne sono idrofobiche dove si trovano gli Ossigeni eterei e gli H legati ai Carboni. I gruppi OH dei C6 esterni sono liberi in realtà e possono formare interazioni polari.
In ambiente acquoso la cavità interna può contenere alcune molecole di acqua legate poco ma a bassa entropia e facilmente spostabili. Nelle loro cavità idrofobe questi carboidrati possono legare composti alifatici o aromatici, composti costituenti l’aroma e medicinali lipofilici.
E’ stato dimostrato che le unità Gamma riescono ad adattare al loro interno una molecola di fullerene C60. Il legame è spinto dal guadagno entalpico ed entropico sulla riduzione nella riduzione della superficie idrofobica acquosa e nel rilascio di molecole d’acqua da dentro la cavità verso la massa del solvente.
In questo modo si sfruttano questi carboidrati ciclici per aumentare la solubilità in acqua di composti idrofobi o di minimizzare l’impatto sugli alimenti di odore o gusto di alcuni additivi.
I complessi delle ciclodestrine sono usate nel campo farmaceutico, negli alimenti e dei prodotti da toilette.
Per esempio le ciclodestrine si ritrovano in prodotti deodoranti in cui le ciclodestrine sequestrano gli odori che in genere sono molecole lipofile.
A questo scopo si introducono sugli Ossigeni 6 dei gruppi sostituenti per modificare la specificità, le proprietà chimiche e fisiche. Le gammaciclodestrine sono le più flessibili per queste sostituzioni.
Si introducono gruppi Idrossipropil e gruppi esteri sulfonici per accrescere la solubilità in acqua e superare le restrizioni nell’uso farmaceutico.
Pagina Originale di Martin Chaplin
CICLODESTRINE – – –
Mostra l’unità costitutiva delle ciclodestrine
– –
Il core idrofobico delle ciclo-destrine è messo in luce dalla visualizzazione della mappa elettrostatica che vede nel centro dell’anello una situazione idrofoba mentre attorno all’anello sono situazioni idrofile.
Dare tempo alla costruzione della mappa da parte del browser.
–
Una molecola anfipatica con una larga superficie idrofobica come il colesterolo porterà la sua parte idrofobica all’interno delle ciclodestrine, realizzando un rapporto di 2 ciclodetrine ad 1 di colesterolo
– – –
Una visione della dinamica molecolare la si può vedere qui