Dalla Chimica Organica conosciamo i meccanismi di eliminazione classica MONOMOLECOLARE e BIMOLECOLARE descritti su questo sito in alcuni articoli.
Meccanismo di eliminazione Monomolecolare e Bimolecolare in generale.
Con Il meccanismo E2 si ha il meccansmo antiperiplanare per cui l’attacco della base e l’uscita del gruppo uscente devono avvenire da posizioni più lontane possibili per minimizzare l’energia dello stato di transizione.
Questo meccanismo porta ad alcheni più ramificati e più stabili termodinamicamente.
In un post del prof. K.P. Gable, che traduciamo in questo articolo, è descritto quello che è comunemente chiamato orientamento anti Zaitev ed un esempio è l’eliminazione di Hofman delle ammine quaternarie.
In generale, una eliminazione che dà il prodotto meno sostituito in eccesso si dice seguire la regola di Hofmann o anti Zaitev.
E’ importante capire perché questo accade. Ci sono varie ragioni che portano un sistema a dare il prodotto di Hofmann.
- Ingombro sterico della base: la base Terzbutilato dà una eliminazione anti Zeitev meglio dell’etilato. Inoltre si ricordi che basi più piccole sono migliori nucleofili e porteranno più prodotto di sostituzione.
- Substrato ramificato. Questo può creare un impedimento sterico alla base che si avvicina all’idrogeno che porta all’elminazione secondo Zeitev. Rallenta la velocità e la produzione del prodotto di Hofman diventa la parte maggiore.
- Cattivo gruppo uscente. Questo porta ad uno stato di transizione in cui il legame C-gruppo uscente è meno rotto, con meno carattere di doppio legame. La conseguenza è minore l’influenza termodinamica dell’alchene che si forma.
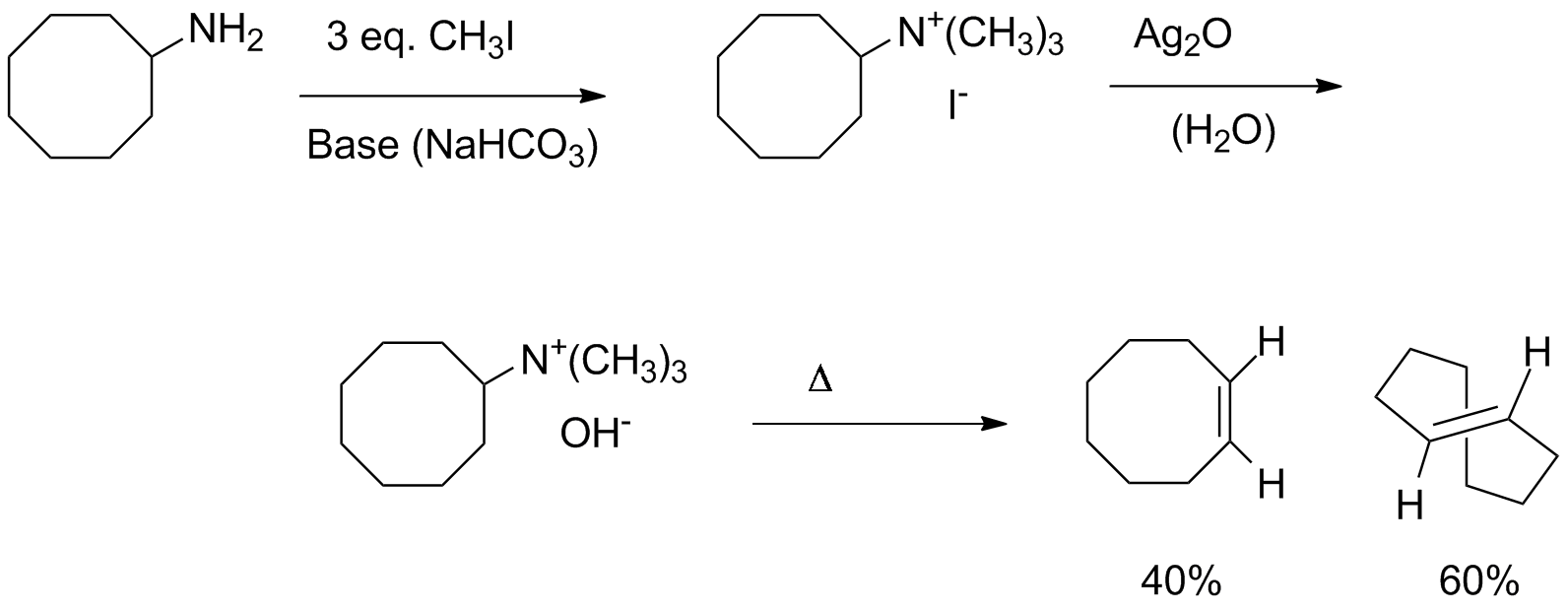
Un eccesso di Iodometano metila completamente l’Azoto con SN2, mentre il bicarbonato neutralizza l’HI che si forma. Quando si aggiunge l’Ossido di Argento precipita AgI e rimane solo OH- come controione. Riscaldando si ha la reazione di eliminazione che porta ai due stereoisomeri nelle quantità date.
Ovviamente l’Eliminazione di Hofmann secondo il meccanismo anti Zeitev è l’esempio migliore e la si può usare per sintetizzare alcheni di scelta che sono meno favoriti termodinamicamante. Questo coinvolge un meccanismo molto differente.
Questo alchene si forma in quantità maggiore, 60%, nonostante sia il termodinamicamente meno favorito con entalpia di formazione in fase gassosa di 20kJ/mole. (dati NIST)
Questo alchene se ne forma il restante 40% nonostante sia i più stabile termodinamicamente con Entalpia di formazione in fase gas -22 kJ/mole (dati NIST)
Questo alchene se ne forma il restante 40% nonostante sia i più stabile termodinamicamente con Entalpia di formazione in fase gas -22 kJ/mole (dati NIST)
In giallo è segnato l’H che porta allo stereoisomero TRANS più energetico; in rosso l’H che porta al CIS termodinamicamente più stabile.
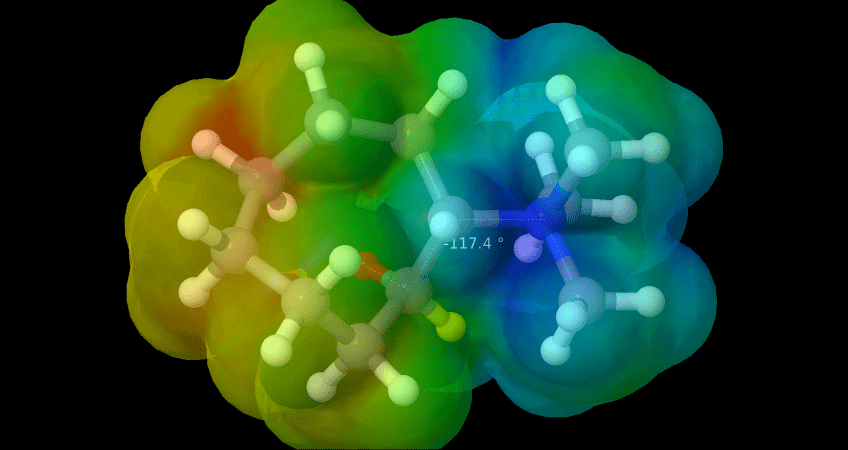
Ora misuriamo l’angolo di diedro tra H ed il gruppo uscente . E’ un angolo che implica un attacco in SIN COPLANARE, mentre l’altro angolo diedro .
Si veda la superficie elettrostatica
Si noti che in questo caso nessun H si trova in conformazione ANTI periplanare, ma solo uno in SIN che si trova in posizione corretta.